Пембролизумаб снижает риск развития отдаленных метастазов или смерти на 40 % по сравнению с плацебо при применении в качестве адъювантной терапии меланомы III стадии
October 7, 2020 8:50 am GMT+0000
Компания MSD и Европейская организация по изучению и лечению рака (EORTC) представили обновленные результаты исследования 3 фазы EORTC1325/KEYNOTE-054 по оценке эффективности пембролизумаба в качестве адъювантной терапии меланомы III стадии после хирургического лечения. Согласно результатам наблюдения на протяжении 3,5 лет, адъювантная терапия пембролизумабом обеспечивает снижение риска развития отдаленных метастазов или смерти на 40 % по сравнению с плацебо (ОР = 0,60 [95 ДИ; 0,49–0,73]; p < 0,001), выживаемость без отдаленных метастазов через 3,5 года составила 65,3 % и 49,4 %, соответственно. Кроме того, пембролизумаб демонстрирует сохраняющееся преимущество по безрецидивной выживаемости (БРВ) при меланоме III стадии по сравнению с плацебо, БРВ через 3,5 года составила 59,8 % в группе пембролизумаба и 41,4 % в группе плацебо (ОР = 0,59 [95% ДИ; 0,49–0,70]; p < 0,001). Преимущество по БРВ и выживаемости без отдаленных метастазов было отмечено во всех подгруппах пациентов, вне зависимости от стадии заболевания (IIIA, IIIB, IIIC), статуса мутации BRAF и наличия экспрессии PD-L1 в опухоли.
«Несмотря на хирургическое лечение, у пациентов с меланомой III стадии может развиться прогрессирование заболевания, а при появлении отдаленных метастазов прогноз зачастую значительно ухудшается», – сообщил Александр Эггермонт (Alexander Eggermont), руководитель исследования, директор по науке онкологического центра принцессы Максимы, Утрехт, Нидерланды. «Обновленные результаты исследования KEYNOTE-054, включая впервые представленные данные по выживаемости без отдаленных метастазировдемонстрируют эффективность адъювантной терапии пембролизумабом при меланоме III стадии, которая снижает риск не только локального рецидива, но и отдаленного метастазирования».
«По данным исследования KEYNOTE-054, адъювантная терапия пембролизумабом демонстрирует долгосрочное снижение риска прогрессирования по сравнению с плацебо, после 3,5 лет наблюдения почти 60 % пациентов живы и у них не наблюдается прогрессирование заболевания», – сообщил д-р Скот Еббингхаус (Scot Ebbinghaus), вице-президент отдела клинических исследований, научно-исследовательского подразделения MSD. «Результаты этого исследования вместе с обновленными данными по выживаемости без отдаленных метастазовдемонстрируют важную роль пембролизумаба в адъювантной терапии меланомы III стадии и свидетельствуют о перспективности дальнейших исследований пембролизумаба при ранних стадиях других типов злокачественных опухолей».
На основании результатов исследования EORTC1325/KEYNOTE-054 пембролизумаб одобрен для адъювантного лечения больных меланомой с поражением лимфатических узлов после хирургического лечения в более чем 70 странах. Обширная программа клинических исследований компании MSD при меланоме и опухолях кожи направлена на удовлетворение существующих потребностей пациентов с онкологическими заболеваниями, путем исследования пембролизумаба в лечении злокачественных опухолей на более ранних стадиях, а также в комбинации с другими противоопухолевыми препаратами.
Дизайн исследования и дополнительные данные подгруппового анализа – EORTC1325/KEYNOTE-054 (тезис доклада № LBA8)
EORTC1325/KEYNOTE-054 (ClinicalTrials.gov, NCT02362594) – это рандомизированное, двойное слепое исследование 3 фазы, финансируемое компанией MSD и проводимое в сотрудничестве с EORTC, которое спланировано для оценки адъювантной терапии пембролизумабом при меланоме III стадии высокого риска рецидива после хирургического лечения по сравнению с плацебо. Первичные конечные точки включали БРВ в общей популяции пациентов, а также БРВ в группе пациентов с экспрессией PD-L1 в опухоли. Вторичные конечные точки включали выживаемость без отдаленных метастазов и общую выживаемость (ОВ) в общей популяции пациентов, а также в группе пациентов с экспрессией PD-L1 в опухоли. Данные по трехлетней БРВ были представлены во время виртуальной научной программы ежегодного онкологического конгресса Американского общества клинической онкологии (ASCO) 2020 года. В соответствии с условиями протокола, исследование продолжается для оценки вторичной конечной точки – ОВ, однако после документированного прогрессирования заболевания в группе плацебо пациентам доступен переход в группу лечения (пембролизумабом).
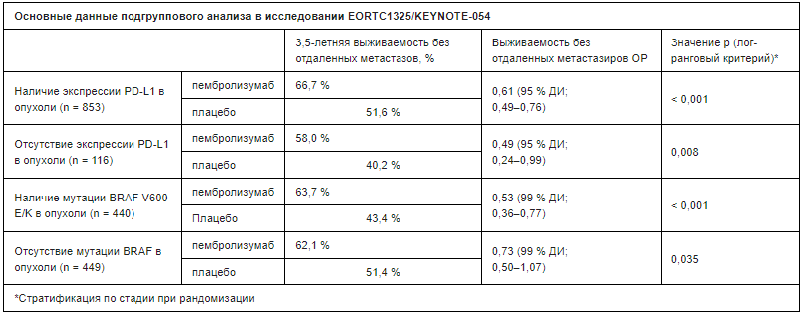
Кроме того, преимущество по выживаемости без отдаленных метастазов в группе лечения пембролизумабом было одинаковым при меланоме IIIA (ОР = 0,64), IIIB (ОР = 0,58) и IIIC стадии (ОР = 0,61), в соответствии с классификацией AJCC-7. Адъювантная терапия пембролизумабом снижает частоту развития отдаленныхметастазов в качестве первого проявления прогрессирования заболевания на 43 % (после 3,5 лет наблюдения: 24,9 % по сравнению с 39,5 %, ОР = 0,57 [95% ДИ; 0,46–0,72]; p < 0,001).
Согласно данным 42-месячного анализа, новых данных по безопасности получено не было. Профиль безопасности пембролизумаба соответствовал данным предшествующих клинических исследований у пациентов с диссеминированной меланомой. В группе лечения пембролизумабом иммуноопосредованные нежелательные явления 3–5 степени тяжести были отмечены у 7,7 % пациентов, а в группе плацебо – у 0,6 % пациентов.
Об EORTC
Европейская организация по исследованию и лечению рака (EORTC) – это академическая организация по клиническим исследованиям, которая объединяет специалистов по всем дисциплинам и всем типам злокачественных опухолей для проведения клинических исследований, задачей которых является улучшение качества и продолжительности жизни пациентов со злокачественными опухолями. Эта организация проводит разного рода исследования, от трансляционных до крупных проспективных многоцентровых клинических исследований 3 фазы по оценке новых вариантов терапии и лечебных подходов, а также качества жизни пациентов. Сеть EORTC насчитывает более 5300 профессионалов из более чем 1000 лечебных учреждений и институтов и более чем 30 стран, штаб-квартира организации находится в Брюсселе, Бельгия.
О меланоме
Меланома – это самая агрессивная форма рака кожи, которая характеризуется неконтролируемым ростом пигментных клеток. Заболеваемость меланомой продолжает увеличиваться на протяжении последних десятилетий – в 2018 году во всем мире было выявлено около 287 000 новых случаев. В США меланома является одним из наиболее часто выявляемых злокачественых заболеваний. Подавляющее большинство случаев смерти от злокачественных опухолей кожи связано именно с этим заболеванием. Ожидается, что в 2020 г. только в США будет выявлено около 100 000 новых случаев и до 7 000 летальных исходов от этого заболевания.
О пембролизумабе
Пембролизумаб – это PD-1 ингибитор, который усиливает способность иммунной системы организма выявлять опухолевые клетки и бороться с ними. Пембролизумаб представляет собой гуманизированное моноклональное антитело, которое блокирует взаимодействие между PD-1 и его лигандами PD-L1 и PD-L2, тем самым активируя Т-лимфоциты, которые могут воздействовать как на опухолевые, так и на здоровые клетки.
Компания MSD обладает крупнейшей в отрасли программой клинических исследований в области иммуноонкологии. В настоящее время пембролизумаб изучается в более, чем 1000 исследованиях, при самых различных злокачественных опухолях и режимах терапии. Целью программы клинического исследования пембролизумаба является изучение его влияния на разные виды опухолей, а также факторов, которые могут предсказать вероятность эффективности терапии пембролизумабом.
Пембролизумаб был впервые зарегистрирован в 2014 году в США для терапии пациентов с неоперабельной и метастатической меланомой, у которых выявлено прогрессирование заболевания после предшествующей терапии. Позже препарат был одобрен для терапии пациентов по 16 показаниям.
Рак головы и шеи – собирательное понятие, под которым понимают группу злокачественных опухолей, развивающихся в тканях гортани, глотки, носа или его пазух, полости рта или из тканей, которые их окружают. Самым распространенным вариантом опухолей головы и шеи является плоскоклеточный рак (ПРГШ). Ежегодно в России раком головы и шеи заболевает более 24 тысяч человек (без учета рака щитовидной железы и рака кожи) Из них более 7,5 тыс. пациентов с распространённым онкологическим процессом. Наиболее значимые факторы риска развития рака головы и шеи – курение табака и злоупотребление алкоголем. К другим факторам риска относится избыточное воздействие солнечного излучения, некоторые инфекции (вирус папилломы человека, вирус Эпштейн-Барр), плохой уход за полостью рта, а также контакт с некоторыми химическими веществами. Мужчины болеют раком головы и шеи в 2-3 раза чаще, чем женщины. Риск выше у людей старше 40 лет. Регистрация нового показания пембролизумаба в ПРГШ открывает доступ к инновационной терапии более чем 5 тыс. пациентов в России.
Рак эндометрия
Рак эндометрия является наиболее распространенным типом рака, который развивается в матке. В 2018 году было подсчитано, что во всем мире было зарегистрировано более 382 000 новых случаев заболевания и почти 90 000 смертей от рака тела матки (эти оценки включают как рак эндометрия, так и саркомы матки).
Меланома
- для лечения взрослых пациентов с неоперабельной или метастатической меланомой;
- в качестве адъювантной терапии у пациентов с меланомой с поражением лимфатических узлов после хирургического лечения.
Немелкоклеточный рак легкого
- в комбинации с химиотерапией, включающей препарат платины и пеметрексед в качестве 1-ой линии терапии у пациентов с метастатическим неплоскоклеточным немелкоклеточным раком легкого при отсутствии мутаций в генах эпидермального фактора роста (EGFR) или киназы анапластической лимфомы (ALK);
- в комбинации с карбоплатином и паклитакселом или альбумин-стабилизированным нанодисперсным паклитакселом в качестве 1-ой линии терапии у пациентов с метастатическим плоскоклеточным немелкоклеточным раком легкого;
- в качестве монотерапии 1-ой линии у пациентов с местно распространенным или метастатическим немелкоклеточным раком легкого с экспрессией PD-L1≥ 1% опухолевыми клетками, определяемой валидированным тестом, при отсутствии мутаций в генах EGFR или ALK;
- в качестве монотерапии для лечения пациентов с распространенным немелкоклеточным раком легкого с экспрессией PD-L1≥ 1% опухолевыми клетками, определяемой валидированным тестом, которые ранее получали терапию, включающую препараты платины. При наличии мутаций в генах EGFR или ALK пациенты должны получить соответствующую специфическую терапию прежде, чем им будет назначено лечение препаратом.
Рак головы и шеи
- в качестве монотерапии или в комбинации с химиотерапией, включающей препарат платины и 5-фторурацил (5-ФУ), в качестве 1-ой линии терапии у пациентов с рецидивирующим или метастатическим плоскоклеточным раком головы и шеи (ПРГШ)
- для лечения пациентов с рецидивирующим или метастатическим плоскоклеточным раком головы и шеи с прогрессированием заболевания во время или после химиотерапии, включающей препараты платины.
Классическая лимфома Ходжкина (кЛХ)
- для лечения взрослых и детей с рефрактерной классической лимфомой Ходжкина или с рецидивом заболевания после трех и более предшествующих линий терапии.
Уротелиальный рак
- для лечения пациентов с местнораспространенным или метастатическим уротелиальным раком, у которых невозможно проведение химиотерапии, включающей цисплатин, с экспрессией PD L1 (комбинированный показатель позитивности (combined positive score, CPS) ≥ 10) по данным валидированного теста, а также у пациентов, которым невозможно проведение химиотерапии любыми препаратами платины, независимо от экспрессии PD L1.;
- для лечения пациентов с местнораспространенным или метастатическим уротелиальным раком, которые ранее получали химиотерапию, включающую препараты платины
Рак желудка
- для лечения пациентов с рецидивирующей местно распространенной или метастатической аденокарциномой желудка или пищеводно-желудочного перехода с экспрессией PD-L1 (комбинированный показатель позитивности (combined positive score, CPS≥ 1) по данным валидированного теста. У пациентов должно быть зарегистрировано прогрессирование заболевания на фоне или после проведения двух и более линий предшествующей терапии, включая химиотерапию фторпиримидинами и препаратами платины, а также, при необходимости, таргетную терапию препаратами анти-НЕR2/nеu.
Злокачественные новообразования с высоким уровнем микросателлитной нестабильности
- для лечения пациентов с распространенными злокачественными новообразованиями с высоким уровнем микросателлитной нестабильности (МSI-H), включая нарушения системы репарации ДНК (dMМR), которые ранее получали терапию
Гепатоцеллюлярный рак
- для лечения пациентов с гепатоцеллюлярным раком (ГЦР), которые ранее получали анти-ангиогенную терапию ингибиторами тирозинкиназ (ИТК).
Рак шейки матки
- для лечения пациентов с рецидивирующим или метастатическим раком шейки матки с экспрессией PD-L1 (CPS≥ 1) по данным валидированного теста при прогрессировании заболевания на фоне или после проведения химиотерапии.
Почечноклеточный рак
- в комбинации с акситинибом в качестве 1-ой линии терапии у пациентов с распространенным почечноклеточным раком (ПКР)
Мелкоклеточный рак легкого
- для лечения пациентов с местно распространенным или метастатическим мелкоклеточным раком легкого (МЛР), которые получали две или более линии терапии
Рак эндометрия
- в комбинации с ленватинибом для лечения пациентов с распространенным раком эндометрия (в случае отсутствия высокой микросателлитной нестабильности (MSI-H) или нарушений системы репарации ДНК (dMMR)) с прогрессированием заболевания после предшествующей системной терапии, которым не показано хирургическое лечение или лучевая терапия.
Об иммуноонкологии
Последние открытия в области иммуноонкологии открывают для пациентов со злокачественными новообразованиями новые возможности в лечении их заболеваний и увеличении продолжительности жизни. Иммуноонкологические препараты усиливают естественную способность иммунной системы бороться с опухолью. В отличие от химиотерапии (которая ингибирует клеточное деление быстрорастущих опухолевых клеток) и таргетной терапии (воздействующей на различные молекулярные мишени на опухолевых клетках) иммуноонкологические препараты воздействуют на различные компоненты иммунной системы, в том числе точки иммунного контроля, в норме отвечающие за регулирование работы иммунной системы.
О компании MSD
Более 125 лет компания MSD создает и производит лекарственные препараты и вакцины для профилактики и лечения опасных заболеваний в мире, реализуя свою миссию по спасению и улучшению жизни людей. MSD – это фирменное наименование компании Merck & Co. Inc., штаб-квартира которой находится в Кенилворте, штат Нью-Джерси, США. Мы реализуем и поддерживаем стратегии, программы и партнерские проекты, которые способствуют повышению доступа пациентов к нашим лекарственным препаратам. Сегодня MSD продолжает оставаться первопроходцем в исследованиях по профилактике и лечению заболеваний, которые угрожают жизни людей и животных, включая онкологические и инфекционные заболевания, такие как ВИЧ-инфекция и лихорадка Эбола. Мы стремимся быть ведущей мировой биофармацевтической компанией, ориентированной на научные достижения. Для получения дополнительной информации вы можете посетить наш сайт: www.msd.ru или связаться с нами в Twitter, Facebook, Instagram, YouTube и LinkedIn.
RU-NON-00244 09.2020
